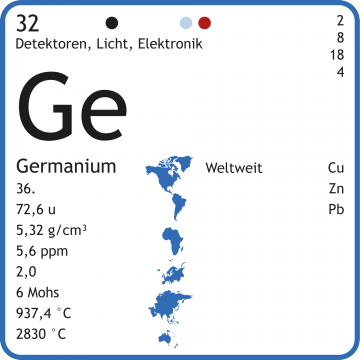
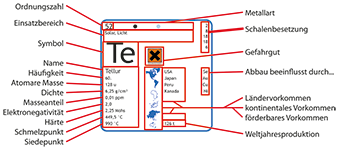
Germanium-Chemie
Nachweis

Darstellung
Generell sind drei Arten der Germanium Gewinnung üblich:
1.) Aus Germanit und Renierit Erzen
2.) Aus Zinkerz Konzentraten
3.) Aus Kohle und Flugasche
Die Trennung erfolgt zunächst aus den Erzen, Kohlen und Flugaschen durch Sieben, magnetische Trennung und unter Nutzung der Dichteunterschiede in der Flotation.
Die Konzentrationen werden so auf über 5% erhöht. An dieser Stelle werden dem Prozess auch Stoffe beigefügt, die in polymetallischen Legierungen Germanium enth…
» Lesen Sie mehr…

Eigenschaften
Germanium steht im Periodensystem in der Serie der Halbmetalle, wird aber nach neuerer Definition als Halbleiter klassifiziert. Elementares Germanium ist sehr spröde und an der Luft bei Raumtemperatur sehr beständig. Erst bei starkem Glühen in einer Sauerstoff-Atmosphäre wird es zu Germanium(IV)-oxid (GeO2) oxidiert. GeO2 ist dimorph und wird bei 1033 °C von der Rutil-Modifikation (CN = 6) in die β-Quarz-Struktur (CN = 4) überführt.…
» Lesen Sie mehr…

Verbindungen
Germanium tritt in seinen Verbindungen sowohl II- als auch IV-wertig auf. Die höhere Beständigkeit weisen dabei die IV-wertigen Moleküle auf. Interessant ist der Aufbau seiner Wasserstoffverbindungen, die analog zu den einfachen gesättigten Kohlenwasserstoffen aufgebaut sind. Das Germanium nimmt hierbei die Rolle des Kohlenstoffatoms ein, welches ebenfalls vierwertige Verbindungen aufbaut. GeH4 ist gasförmig und wird als Monogerman bezeichnet. In der Kohlenstoffchemie w&…
» Lesen Sie mehr…